Преди да започнем директно да се запознаем с понятията, свързани с оловната батерия, нека започнем с нейната история. И така, френски учен на име Никола Гатеро през 1801 г. отбелязва, че при тестовете за електролиза съществува минимално количество ток, дори когато има изключване на основната батерия. Докато през 1859 г. учен на име Гатсън разработва оловно-киселинна батерия и това е първата, която се зарежда чрез преминаване на обратен ток. Това беше първоначалната версия на този вид батерия, докато Faure след това добави много подобрения към това и накрая, практичният тип оловно-киселинна батерия беше изобретен от Анри Тудор през 1886 г. Нека да проведем по-подробна дискусия за този вид батерия , работа, видове, конструкция и предимства.
Какво е оловна батерия?
Оловно-киселинните батерии са класифицирани като акумулаторни и вторични батерии. Въпреки минималните пропорции на батерията в енергията към обема и енергията към теглото, тя притежава способността да доставя увеличени токове на пренапрежение. Това съответства на това, че оловните киселинни клетки притежават голямо количество тегловни пропорции.
Това са батериите, които използват оловен пероксид и гъбен олово, за да преобразуват химическата енергия в електрическа. Те се използват най-вече в подстанции и енергийни системи поради причината, поради която имат повишени нива на напрежение в клетките и минимални разходи.
Строителство
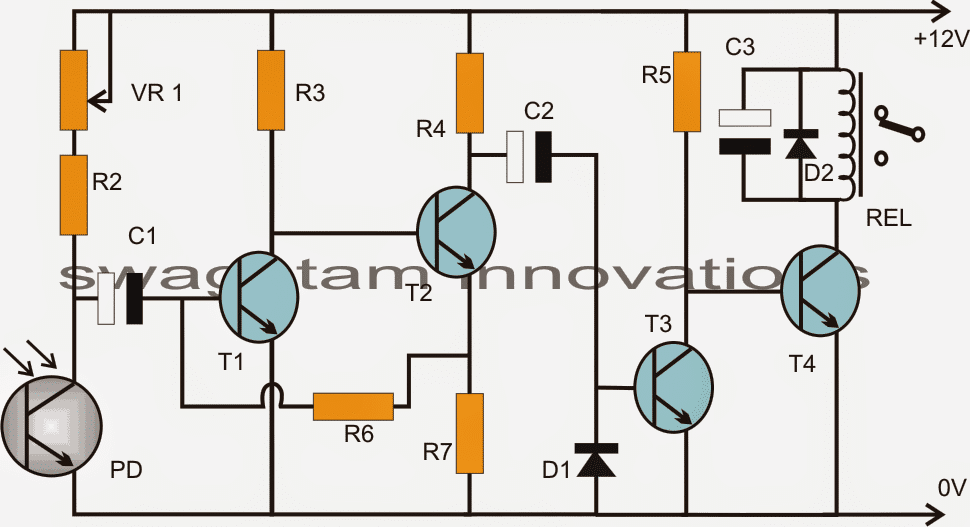
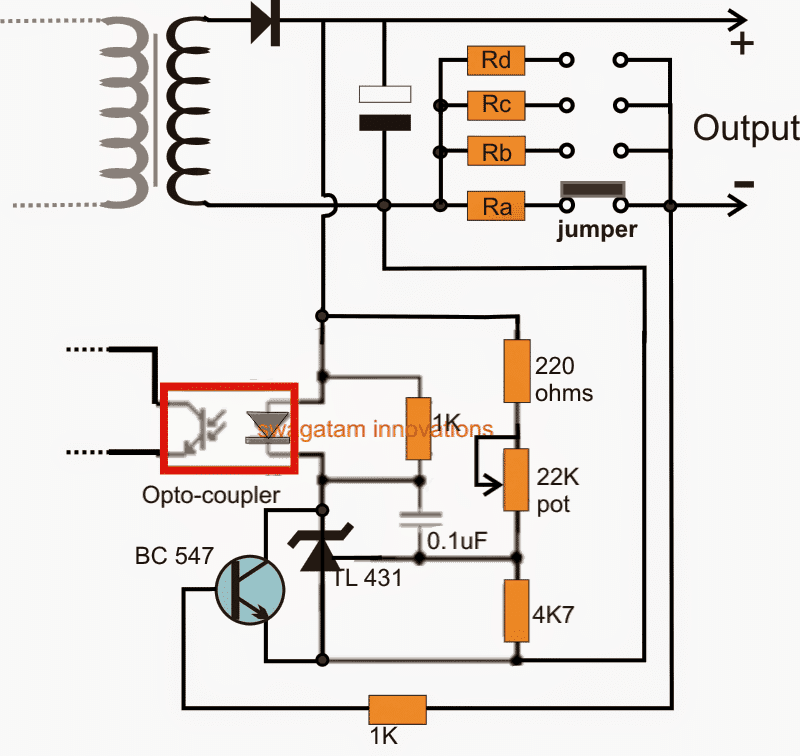
В конструкция на оловна батерия , чиниите и контейнерите са най-важните компоненти. Разделът по-долу предоставя подробно описание на всеки компонент, използван в конструкцията. The диаграма на оловна батерия е

Диаграма на оловно-кисели батерии
Контейнер
Тази част на контейнера е изработена от ебонит, дърво, покрито с олово, стъкло, твърда гума, изработена от битумния елемент, керамични материали или кована пластмаса, които са поставени отгоре, за да се премахне всякакъв вид електролитен разряд. Докато в долната част на контейнера има четири ребра, където две са поставени върху положителната плоча, а останалите върху отрицателната плоча.
Тук призмата действа като основа за двете плочи и освен това предпазва плочите от късо съединение. Компонентите, които се използват за конструкцията на контейнера, трябва да са без сярна киселина, те не трябва да се огъват или да пропускат и да не съдържат никакви примеси, което води до увреждане на електролитите.
Плочи
Плочите в оловно-киселинната батерия са конструирани по различен начин и всички са изградени от подобни типове решетка, която е изградена от активни компоненти и олово. Решетката е от решаващо значение за установяване на проводимостта на тока и за разпространение на равни количества токове към активните компоненти. Ако има неравномерно разпределение, тогава ще има разхлабване на активния компонент. Плочите в тази батерия са два вида. Те са от планта / оформени плочи и Faure / залепени плочи.
Оформените плочи се използват главно за статични батерии и те също са тежки и скъпи. Но те имат дълга трайност и те не са лесно склонни да загубят активните си компоненти дори при непрекъснати процеси на зареждане и разреждане. Те имат минимално съотношение между капацитета и теглото.
Докато залепеният процес се използва предимно за конструиране на отрицателни плочи, отколкото на положителни плочи. Отрицателният активен компонент е донякъде сложен и те изпитват леко изменение в процесите на зареждане и разреждане.
Активен компонент
Компонентът, който активно участва в процесите на химическа реакция, които се случват в батерията главно по време на зареждане и разреждане, се нарича активен компонент. Активните компоненти са:
- Оловен пероксид - Той образува положителен активен компонент.
- Гъбесто олово - Този материал образува отрицателния активен компонент
- Разредена сярна киселина - Това се използва главно като електролит
Разделители
Те са от тънки листове, които са изградени от пореста гума, покрито оловно дърво и стъклени влакна. Разделителите са разположени между плочите, за да осигурят активна изолация. Те имат набраздена форма от едната страна и гладко покритие от останалите ръбове.
Ръбове на батерията
Той има положителни и отрицателни ръбове с диаметър 17,5 mm и 16 mm.
Принцип на работа на оловна батерия
Тъй като сярната киселина се използва като електролит в батерията, когато тя се разтвори, молекулите в нея се диспергират като SO4-(отрицателни йони) и 2Н + (положителни йони) и те ще имат свободно движение. Когато тези електроди се потопят в разтворите и осигурят захранване с постоянен ток, тогава положителните йони ще се движат и ще се движат към посоката на отрицателния ръб на батерията. По същия начин отрицателните йони ще се движат и ще се движат към посоката на положителния ръб на батерията.
Всеки водород и сулфатни йони събират един и двуелектронни и отрицателни йони от катода и анода и те имат реакция с вода. Това образува водород и сярна киселина. Докато развитите от горните реакции реагират с оловен оксид и образуват оловен пероксид. Това означава, че по време на процеса на зареждане оловният катоден елемент остава като олово, докато оловният анод се формира като оловен пероксид, който е тъмнокафяв на цвят.
Когато няма DC захранване и след това по времето, когато между електродите е свързан волтметър, той показва потенциалната разлика между електродите. Когато има връзка на проводник между електродите, ще има преминаване на ток от отрицателната към положителната плоча чрез външна верига, което означава, че клетката притежава способността да осигурява електрическа форма на енергия.
И така, това показва оловна батерия работи сценарий.
Различни видове
The типове оловни батерии са главно категоризирани в пет вида и са обяснени подробно в долния раздел.
Наводнен тип - Това е конвенционалният тип запалване на двигателя и има акумулаторна батерия. Електролитът има свободно движение в клетъчната секция. Хората, които използват този тип, могат да имат достъп до всяка клетка и могат да добавят вода към клетките, когато батерията изсъхне.
Запечатан тип - този вид оловна батерия е само малка промяна в наводнения тип батерия. Въпреки че хората нямат достъп до всяка клетка в батерията, вътрешният дизайн е почти подобен на този наводнен тип. Основната вариация при този тип е, че има достатъчно количество киселина, която издържа на плавен поток от химични реакции през целия живот на батерията.
Тип VRLA - Те се наричат Оловно-киселинни батерии, регулирани от клапани които също се наричат запечатан тип батерии. Процедурата за контрол на стойността позволява безопасното развитие на Oдвеи Ндвегазове по време на зареждане.
AGM Тип - Това е тип батерия Absorbed Glass Matte, която позволява на електролита да спре в близост до материала на плочата. Този вид батерия увеличава ефективността на процесите на разреждане и зареждане. Те се използват особено в силовите спортове и приложенията за иницииране на двигатели.
Тип гел - Това е мокрият вид оловно-киселинен акумулатор, при който електролитът в тази клетка е свързан със силициев диоксид, което прави втвърдяването на материала. Стойностите на напрежението на презареждане на клетката са минимални в сравнение с други видове и също има по-голяма чувствителност.
Химична реакция на оловна батерия
Химичната реакция в акумулатора се случва главно по време на методите за разреждане и презареждане и в процеса на разреждане се обяснява по следния начин:
Когато батерията е напълно разредена, тогава анодът и катодите са PbOдвеи Pb. Когато те са свързани чрез съпротивление, батерията се разрежда и електроните имат обратния път по време на зареждането. Hдвейони имат движение към анода и те се превръщат в атом. Достига се с PbOдве, като по този начин се образува PbSO4който е бял на цвят.
По същия начин сулфатният йон има движение към катода и след достигането йонът се формира в SO4. Реагира с олово катод като по този начин се образува оловен сулфат.
PbSO4+ 2H = PbO + HдвеИЛИ
PbO + HдвеТАКА4= PbSO4+ 2НдвеИЛИ
PbOдве+ НдвеТАКА4+ 2Н = PbSO4+ 2НдвеИЛИ

Химична реакция
По време на процеса на презареждане катодът и анодите са във връзка с отрицателните и положителните ръбове на захранването с постоянен ток. Положителните H2 йони се движат по посока на катода и те получават два електрона и се образуват като H2 атом. Той претърпява химическа реакция с оловен сулфат и образува олово и сярна киселина.
PbSO4+ 2НдвеO + 2H = PbSO4+ 2 НдвеТАКА4
Комбинираното уравнение за двата процеса е представено като

Процес на разреждане и зареждане
Тук стрелката надолу показва разряд, а стрелката нагоре показва процеса на презареждане.
Живот
Оптималната функционална температура за оловно-киселинната батерия е 250С, което означава 770Е. Увеличението на температурния диапазон съкращава дълголетието. По правило, за всяко повишаване на температурата с 80 ° C, намалява времето на полуразпад на батерията. Докато батерия с регулирана стойност, която функционира на 250C има a живот на оловната батерия от 10 години. И когато това се работи на 330C, той има само 5 години живот.
Приложения за оловни батерии
- Те се използват в аварийно осветление, за да осигурят захранване на помпите за картер.
- Използва се в електрически двигатели
- Подводници
- Ядрени подводници
Тази статия обяснява принципа на работа на оловно-киселинните батерии, видовете, живота, конструкцията, химическите реакции и приложенията. Освен това знайте кои са предимства на оловна батерия и недостатъци в различни домейни?